慢性伤口愈合困难,一直是临床治疗中的一大难题。传统疗法不仅恢复过程缓慢,还常伴有生物相容性差、炎症反应持续以及瘢痕形成等问题,给患者带来极大困扰。近年来,脂肪源性干细胞外泌体(ADSC-exo)因其具备抗炎、免疫调节和促进组织再生的潜力,成为组织修复领域备受关注的新型治疗工具。然而,直接注射外泌体存在半衰期短、易被体内快速清除、难以靶向聚集以及功能易丧失等局限,严重制约了其临床应用效果。
因此,如何构建一种高效、稳定的递送系统,以延长外泌体在体内的活性与作用时间,并精准释放其修复潜能,已成为科研界的研究热点和突破口。
近日,东南大学数字医学工程全国重点实验室张天柱教授团队设计并验证了一种多功能G-Avs贴片,它不仅能实现外泌体的持续释放,还能有效调控炎症、促进组织再生,为慢性伤口治疗带来全新思路。

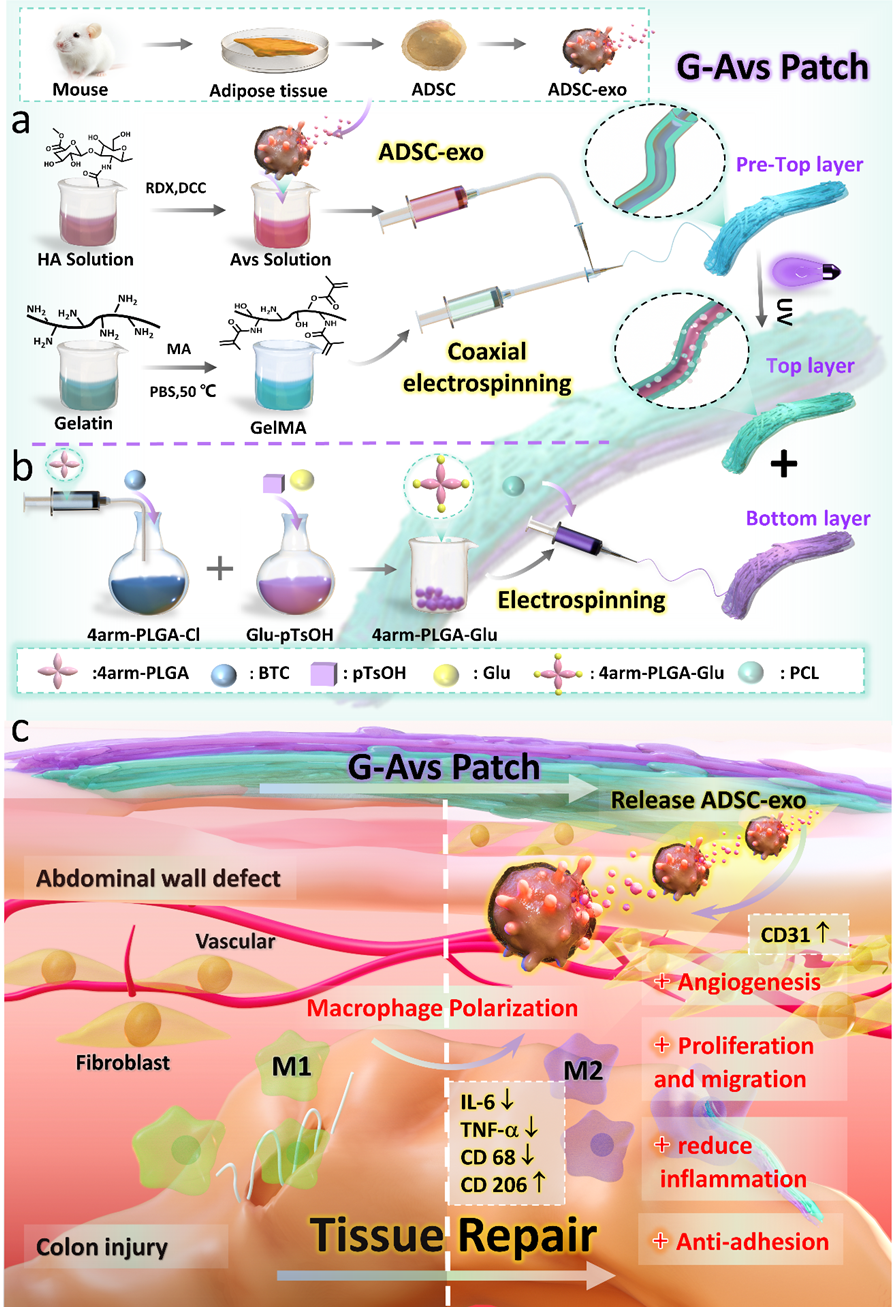
补片的上层采用先进的同轴静电纺丝技术制备,将脂肪源性干细胞外泌体(ADSC-exo)与透明质酸(HA)共同封装在甲基丙烯酰化明胶(GelMA)纳米纤维中,形成稳定的核-壳结构,实现外泌体的持续释放,显著提升其生物活性和治疗效果。
补片的下层则由4臂聚乳酸-羟基乙酸共聚物(4aPLGA)-Glu与聚己内酯(PCL)构成静电纺丝疏水膜,具备润滑且抗污的表面特性,不仅有效防止蛋白质吸附,还能为组织提供良好的机械支撑,避免术后粘连。
在大鼠模型实验中,G-Avs补片展现出强大的组织修复能力:不仅能显著促进细胞增殖、血管生成,还可引导巨噬细胞向M2型极化,有效减轻炎症反应,加速伤口愈合。通过转录组分析进一步揭示,该补片可通过激活代谢相关通路、抑制免疫与炎症信号通路,全面改善细胞能量代谢,为组织再生提供有力支持。
综合体外与体内研究结果,G-Avs补片凭借其双层功能设计,在肠道及腹壁缺陷修复中展现出广阔的临床应用潜力,为慢性伤口及术后组织修复提供了全新的解决方案。有巨大的临床转化潜力。
相关成果以“Adipose-Derived Stem Cell-derived Exosomes Encapsulated Patch for Modulating Inflammation and Promoting Tissue Regeneration”为题,发表在《ACS Nano》上。东南大学生物科学与医学工程学院博士生陶英华为该论文第一作者,东南大学数字医学工程全国重点实验室张天柱教授和南京大学医学院附属南京鼓楼医院普外科殷祎医师为共同通讯作者。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.4c16058

